invecchiamento della retina la fotobiomodulazione funziona ?

EYE of the needle
Marzo 19, 2022
Astigmatismo e Cataratta – Correzione con il Cristallino Torico
Aprile 10, 2022
Studio Scientifico In Ospedali USA
LumiThera, ditta produttrice dello strumento Valeda, annuncia nel marzo 2022 che lo studio clinico USA LIGHTSITE III ha raggiunto l’obiettivo di efficacia nel migliorare la vista nei soggetti con degenerazione maculare secca legata all’età.
LumiThera ha reso noti i risultati provvisori a un anno dello studio clinico multicentrico USA LIGHTSITE III del trattamento di fotobiomodulazione in pazienti con degenerazione AMD secca. I pazienti hanno ricevuto un trattamento con una luce diodo specifica ogni 4 mesi per 24 mesi. L’analisi ha incluso 91 occhi nel gruppo di trattamento e 54 occhi nel gruppo di controllo. I dati hanno mostrato un miglioramento significativo della vista dopo un anno nel gruppo di trattamento. Lo studio continuerà a trattare e seguire i soggetti fino 24 mesi come previsto
L’uso della fotobiomodulazione (PBM), in precedenza definita terapia della luce di basso livello energetico, comporta un uso mirato di lunghezze d’onda selezionate dalla luce visibile al vicino infrarosso (NIR) luce (500–1.000 nm). Il raggio è prodotto da un laser o una sorgente luminosa non coerente come i diodi emettitori di luce.
La fotobiomodulazione può essere applicata a tessuti selezionati per produrre effetti cellulari benefici che portano a miglioramento del metabolismo a livello cellulare.
Il meccanismo alla base di questi benefici suggerisce il coinvolgimento dell’enzima chiave citocromo C ossidasi all’interno dei mitocondri.
I mitocondri sono organelli all’interno delle cellule con funzioni energetiche e di produzione di molecole essenziali per la vita della cellula.
sono organelli all’interno delle cellule con funzioni energetiche e di produzione di molecole essenziali per la vita della cellula.
Gli effetti benefici del PBM sarebbero legati all’aumento della generazione di energia mitocondriale e ad uno stimolo “al rinnovo e riparazione” di alcune componenti della cellula.
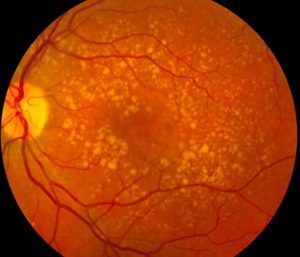
Drusen, formazioni multiple giallastre
Gli studi riportano una riduzione nel tempo delle drusen, accumuli di materiale “di scarto” del metabolismo delle cellule visive e del loro strato di supporto, l’epitelio pigmentato retinico. Le drusen sono considerate lesioni che predispongono allo sviluppo delle degenerazione maculare senile.

Riduzione della quantità di lesioni drusenoidi
Il Trattamento
Le sessioni durano pochi minuti e prevedono la esposizione della retina alla luce emessa dal diodo dello strumento, in base a parametri predeterminati dal protocollo. Il trattamento non è doloroso. Le sessioni vanno ripetute ogni circa 4 mesi.
La Degenerazione Maculare Secca legata all’età 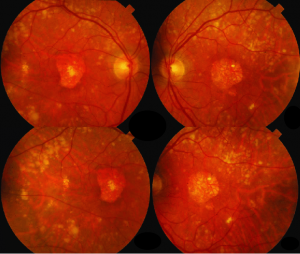
L’AMD è una delle principali cause di perdita della vista per le persone di età pari o superiore a 65 anni. Perdere la visione centrale può rendere progressivamente negli anni più difficile vedere i volti, guidare o fare lavori ravvicinati come leggere, cucinare o sistemare le cose in casa. Si stima che la prevalenza complessiva di AMD aumenti di 7 volte con l’età, dal 4,2% in quelli di età compresa tra 45 e 49 anni, al 27,2% in quelli di età compresa tra 80 e 85 anni. Buona parte di questa patologia è molto lenta e non raggiunge livelli critici di perdita di autonomia personale. La degenerazione si manifesta come una progressiva perdita di nitidezza e di “slavatura” delle immagini, prima per vicino e poi anche per lontano, che fa pensare ad una cataratta. La patologia non porta alla cecità, nel senso di buio completo della vista, ma rende difficili le normali attività della vita quotidiana. La conferma diagnostica necessita di esami oculistici specialistici. Attualmente non c’è una terapia efficace per prevenire o fermare l’evoluzione peggiorativa. La terapia con iniezioni di farmaci anti-angiogenici non si applica a questa forma, ma a quella “umida” o neovascolare, che ne rappresenta la complicazione in un quarto dei casi.
Speranze
Il trattamento di fotobiomodulazione è stato introdotto da alcuni anni, ma non si è mai diffuso in modo pieno per la mancanza di dati scientifici solidi e convincenti.
Lo studio LIGHTSITE III dà maggiori incoraggiamenti sulla efficacia del trattamento e pone le premesse per un allargamento ed approfondimento degli studi sia in senso clinico reale che sui tessuti in laboratorio
Cautele
Il laser per la fotobiomodulazione ha il marchio CE di commercializzazione per l’Europa, ma non è approvato per l’uso dalla Food & Drug Administration (FDA) negli Stati Uniti. Questo significa che lo strumento possiede caratteristiche di sicurezza secondo le norme europee, ma non c’è nessuna garanzia attuale di efficacia clinica. Negli USA, la FDA verifica l’efficacia sulla salute e gli effetti collaterali prima di consentire trattamenti e strumentazioni nuove. Prima del via libera in USA passeranno quindi alcuni anni.
L’efficacia include test su aspetti diversi della vista e delle anomalie della struttura della retina. Si verificano fattori di confusione nei risultati sia positivi che negativi, la necessità di un numero di pazienti maggiore, la opportunità di modificare i protocolli di trattamento. Importanti sono gli effetti collaterali. Un trattamento può essere innocuo a breve termine e non esserlo a distanza di tempo.
LumiThera Inc.,è un’azienda di dispositivi medici di Seattle, con intenti commerciali. Ha ovviamente e legittimamente interesse a accentuare al massimo i risultati positivi.
Conclusione
Con queste limitazioni sulle dimostrazioni di efficacia effettiva, il trattamento è disponibile in Italia in alcuni centri. Chi decide di sottoporsi senza attendere ulteriori conferme sa che non ci sono ancora certezze definitive.